新変異株”KP.3”の出現によりコロナ感染者が増加していることから、コロナの治療薬が話題になることも多い。入院や死亡を防ぐことができれば、服用したいところであるが、3月に支援策が終了し、医療費が自己負担となったことから高額な治療薬に二の足を踏む患者も多い。
ところで、わが国で使用可能なコロナ治療薬の中では、ラゲブリオ(モルヌピラビル)が最もよく処方されている。2023年の売り上げは1,487億円で、全医薬品のなかでも、キイトルーダに次いで第2位であった。ラゲブリオの1日薬価は18,862円なので、5日間投与すると94,000円、3割負担で自己負担額は28,200円である。
MSD製薬HPより
ラゲブリオは米国エモリー大学発のベンチャー会社によって見いだされ、MSD社が開発した薬剤である。RNAポリメラーゼを阻害することにより、ウイルスRNAの配列に変異を導入して、ウイルスの増殖を抑制する。動物実験で、催奇性や胎児致死がみられたことより、妊婦や妊娠の可能性のある女性には禁忌である。
ラゲブリオの申請は、日本を含む20カ国が参加したMOVe-OUT試験の結果に基づいて行われ、わが国では2021年12月24日に特例承認された。MOVe-OUT試験は、軽症・中等症でワクチン接種歴のない成人患者を対象としており、症例が登録されたのが2021年5月から9月だったので、対象となった流行株はミュー株、デルタ株、ガンマ株で、オミクロン株による感染は含まれていない。(表1)
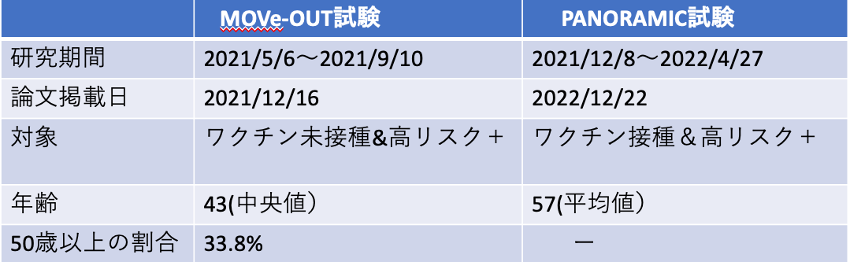
表1 ラゲブリオに対する無作為割付試験の概要
1,550例を目標症例としたが、中間解析の結果、データモニタリング委員会から新規症例の組み入れ中止が勧告されたことから、762例の結果で審査がおこなわれた。主要評価項目である無作為割付化後29日までの入院あるいは死亡した患者の割合は、ラゲブリオ群では28/385(7.3%)で、プラセボ群の53/377(14.1%)と比較して相対リスクとして50%の減少がみられた(p=0.001)。(表2)
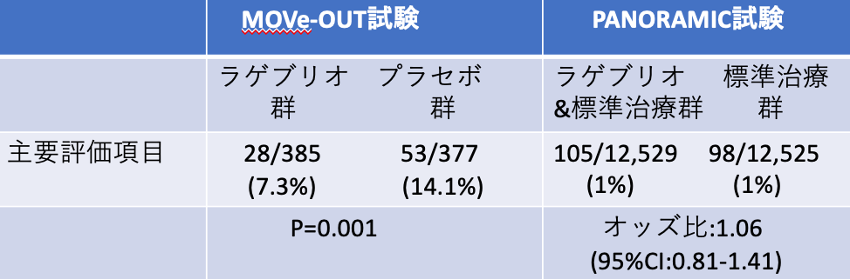
表2 ラゲブリオに対する無作為割付試験の結果
N Engl J Med 2022; 386:509 Lancet. 2023; 401:281
困惑することに、11月末になって50%の効果が30%に下方修正された。本試験は2021年の5月6日に開始され、9月10日までに登録された症例によって中間解析されたが、最終的に患者登録が終了したのは10月2日で、治験に参加した総患者数は1,433人であった。患者数が増えた結果、効果が50%から30%に減少したというのである。
最終解析では、ラゲブリオ群の入院あるいは死亡患者の割合は、48/709(6.8%)でプラセボ群の68/699(9.7%)と比較して30%の減少しかみられなかった。
このあたりの事情について、筆者は、2022年1月25日付けの全国保険医新聞に以下の記事を投稿している。
中間解析以降に追加された症例について両群を比較すると、ラゲブリオ群の入院あるいは死亡した患者の割合は20/324(6.2%)で、プラセボ群の15/322(4.7%)と比較してかえって多かった。中間解析後の症例を加えたことにより、両群の差が縮小した理由に関しては、審議結果報告書では不明とされている。中間解析までの症例と追加症例の流行株の違いが影響したかもしれない。第6波の主流となるオミクロン株での重症患者が少ないことや、治験には日本人が8人しか含まれていないことを考慮すると、市販後調査でも有効性が科学的に検証できる仕組みを整えておくことが望まれる。
英国では、2021年11月に条件付き販売承認がラゲブリオに与えられたが、12月から、標準治療への上乗せ効果を検討するために、PANORAMIC試験が開始された。
研究対象は、症状出現後5日以内の成人で、多くは、標準治療として解熱剤が投与されたが、超高リスクの患者のなかには、モノクローナル抗体やレムデシビルのような抗ウイルス薬の投与を受けた患者もいる。MOVe-OUT試験とは異なり、99%はワクチン接種歴があり、流行株はオミクロン株であった。
主要評価項目である無作為化28日以内の入院あるいは死亡した患者の割合は、ラゲブリオ&標準治療群は105/12,529(1%)で、標準治療群の98/12,525(1%)との間に差は見られなかった。EMA(欧州医薬品庁)は、PANORAMIC試験の結果をうけて、ラゲブリオの販売承認を取り消した。取り消しにあたっては、MOVe-OUT試験に対する下記の評価がその根拠となった。
中間解析以降のMOVe-OUT試験の結果では、入院または死亡の発生に2群間で差がみられていない。中間解析の結果は、早期のパンデミック期における、ワクチン未接種患者を対象としたものであり、現在のヨーロッパの集団に外挿することはできない。
まさに、筆者が全国保険医新聞に記したことと同じ懸念でもって、EMAはラゲブリオの承認を取り消したのだ。
今年になって、MSD社は日本におけるラゲブリオの市販後調査の結果を報告した。解熱剤などの標準治療にラゲブリオが上乗せされたのは、PANORAMIC試験と同様である。
95%の患者は、高血圧や糖尿病などのリスク因子を持ち、84%にはワクチン接種歴があった。外来治療を行なった2,006人のうち、ラゲブリオの投与開始後29日までに、入院あるいは死亡した患者は47人(2.3%)であった。しかし、対照群がないのでのラゲブリオの効果については評価できていない。
2022年には56.84億ドル(8,000億円)あったラゲブリオの売り上げも、世界的なコロナ流行の終息に加え、ヨーロッパでの販売中止が影響して、2023年には4分の1の14.28億ドル(2,000億円)に激減した。2023年の日本におけるラゲブリオの売り上げは1,487億円と全体の7割を占め、日本はMSD社にとっては残された草刈り場なのであろう。
7月16日に開催された東京都医師会定例記者会見で、尾﨑会長は、
“治療薬を飲みますかと患者にきいても、ラゲブリオとパキロビットは3割負担で3万円、そんなに高価なら我慢しますという話になってしまう。せめて感染者数が増加する夏場だけでもいいので、コロナ治療薬の自己負担が3000~5000円程度で済むような対応を国や都にお願いしたい。
と提言しているが、ラゲブリオやパキロビッドの効果を問題にすることが先であろう。
【関連記事】