daboost/iStock
EBM(Evidence-Based Medicine)の概念には賛否両論があります。コロナパンデミック以降は、この概念に疑問を持つ医師が増加してきた印象があります。しかしながら、EBMの概念を超えるものは現時点では提示されていないため、この概念をベースにして「コロナワクチンと有害事象との因果関係」を評価していくことが現時点では妥当と私は考えます。
ただし、EBMの根拠となる疫学的手法には限界があることは事実であり、限界があることを踏まえた上で結果を解釈することが重要です。また、ASA声明で述べられているように、1つのp値のみで科学的決定を下すことは適切ではなく、複数のエビデンスより多面的に検証することが大切です。
今回の論考を書くに当たり、以下の資料を参考にしました。(参考資料1、参考資料2、参考資料3、参考資料4、参考資料5)
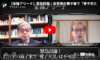
EBMではエビデンスレベルが提示されており、レベルの高い研究ほど信頼できる研究とされます。エビデンスレベルの定義には様々なものが提案されていますが、上記の参考資料より、以下のようにエビデンスレベルをまとめてみました。
【エビデンスレベル】
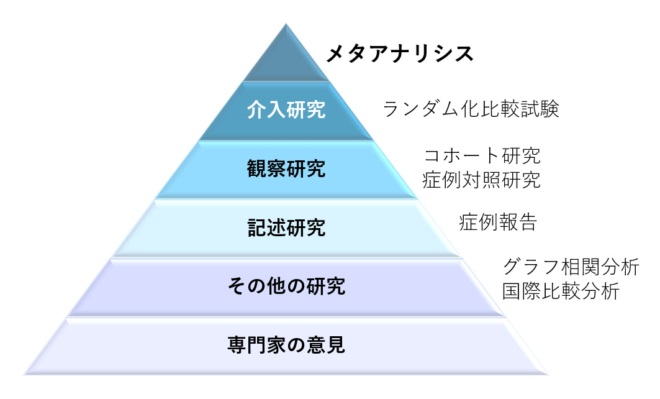
レベル1.システマティックレビュー、メタアナリシス
レベル2a.介入研究:ランダム化比較試験(RCT)
レベル2b.介入研究:非ランダム化比較試験
レベル3a.観察研究:コホート研究など
レベル3b.観察研究:症例対照研究、SCRIデザインなど
レベル3c.免疫組織学的研究など
レベル4.記述研究:症例報告など
レベル5.エコロジカル研究(国別の比較など)、各種グラフ相関分析
レベル6.専門家の意見
番外. 基礎研究(動物実験、In vitro研究)
現時点で、学会や論文でコロナワクチン接種後の副反応疑い事例が極めて多く報告されています。しかしながら、そのエビデンスレベルはレベル4にすぎません。つまり、いくらたくさん症例が報告されていようともエビデンスとしては不十分なのです。ただし、免疫組織学的手法を用いた症例報告は価値が高いため、私の個人的見解に基づきレベル3としました。
なぜ症例報告ではエビデンスとして不十分なのかと言いますと、一つ一つに事例では、因果関係のある事例なのか、偶発的事例なのかを原則的に判断できないからです。WHOの因果関係評価マニュアル(p.10)では次のように記載されています。
At the individual level it is usually not possible to establish a definite causal relationship between a particular AEFI and a particular vaccine on the basis of a single AEFI case report.
AEFI : adverse event following immunization
個人レベルでは1件の接種後有害事象報告に基づいて、特定の有害事象と特定のワクチンとの間の明確な因果関係を立証することは通常不可能である。
コロナワクチンと有害事象との因果関係を検証するには、レベル3以上の研究が必要です。日本の副反応検証の最大の問題点は、レベル3以上の研究がほとんど無いということです。コホート研究としては、Takeuchiらの論文があるだけであり、しかもその研究は一つの都市に限定した規模の小さいコホート研究なのです。
「国によるコロナワクチン副反応の検証は不十分だ」という主張は、しばしば耳にしますが、では具体的に何をするべきかについて的確に提言できている人は多くいません。
日本においての個々の症例を集め直して検討し直すということは大切ですが、それで検証が十分になるわけではありません。繰り返しますが、レベル3以上の研究をしないと学問の世界では評価されません。2011年、 米国FDAは因果関係評価の大転換を図り、 評価の際には疫学的分析を重視するようになりました。
厚労省は、なぜ「重大な懸念はない」と判断するのか?
この判断を下すには、日本のデータを用いた疫学的分析が必要です。報告バイアスがある報告事例データのみより判断することは適切ではありません。つまり、死亡報告事例が多ければ「重大な懸念がある」と判断されるわけではないのです。また、救済認定された死亡者数は900人を超えていますが、厳密な因果関係を必要としない認定であるため、これも判断の根拠とはなりません。
PMDAがシグナル検出を実施しているようなのですが、そのデータはほとんど公表されていません。 2022年1月末時点のデータ分析が公表されているのみです。オミクロン株以降の日本においてのコホート研究は実施されておりません。日本の高齢者医療の在り方は欧米とは異なるため、欧米のデータを用いた疫学的分析のみでは根拠として不十分です。日本においての重大な懸念の有無を問題にしているわけですから、日本のデータを用いた分析が必須です。
したがって、厚労省の「重大な懸念はない」という主張の根拠は全く不十分です。厚労省は、「専門家による審議会の検証によるものだ」と説明していまが、その具体的な根拠を明らかにするべきです。
どうすれば厚労省の判断を覆すことができるのか?
審議会の判断の根拠を厚労省に質すことが一つの方法です。更に言えば、PMDAで実施された2024年~2025年のデータ分析の有無を質問することも有効です。具体的な分析結果が提示できなければ、科学的根拠もないのに厚労省は、「重大な懸念はない」と主張していることになります。審議会のメンバーがどれだけ優秀な人であったとしても、日本のデータを用いた疫学的分析をせずにリスクを判断することはできません。
他の方法としては、レベル3以上の日本においてのエビデンスを厚労省に突き付けることです。しかし、これは容易なことではありません。「接種群の死亡率と未接種群の死亡率を比較すればよい」と主張している人もいますが、バイアスが適切に補正されていませんと、比較しても意味がありません。
コロナワクチンでは、「全身状態が悪い人には接種しない」ことが推奨されました。しかし、このことがどの程度まで遵守されたのかは調査されていません。したがって、全身状態の悪い人の割合が各群で何%なのかは不明なのです。この割合が不明な状態で、死亡率を比較しても何の意味もありません。何故ならば、全身状態の悪い人の割合が大きい群の方が死亡率が高くなる蓋然性が高いからです。この問題は、以前の論考で解説しました。
疫学分析の他の方法としては、SCRIデザインなどの偶発性の検証があります。コホート研究には限界があり、それを補完できるのが偶発性の検証なのです。この問題は、英語論文にまとめて発表しています。ただし、日本では報告バイアスがないようにデータを収集することが難しいため、偶発性の検証は現実には困難です。
ただし、接種後死亡者の全数調査は自治体の協力があれば、ある程度までは偶発性の検証が可能です。全数調査であれば報告バイアスはなくなります。
私は、札幌市が提供してくれたデータを用いて、論考1と論考2を公開しています。札幌市は、死因のデータは提供してくれませんでした。このデータが提供されれば、更に詳細な分析が可能となります。政府であればこれらのデータの入手は容易ですから、政府が接種後死亡の全数調査をするべきです。
疫学的分析の問題点を提示することも有用
現在実施されている疫学的手法には限界があり、検証として不十分であることを指摘することも有用です。既に述べたように関連性の検証のために主に実施されているコホート研究には、原理上の限界がいくつかあり、改善の余地があります。この問題も英語論文で指摘しました。
まず、コホート研究で有意差が認められなかった場合には、関連性がなかったと解釈することはできません。
次に、この手法には、未接種群の有害事象の発生率が高い場合には、有意差が生じにくくなるという原理的欠陥があります。具体例を一つ挙げれば、流産です。10,000件/100万接種という非常に高い発生率でもコホート研究では有意差が認められないのです。したがって、コホート研究で有意差が認められない場合に、有害事象の発生率は無視できるほど発生率が低いと必ず解釈できるわけではないのです。
一流のジャーナルであっても、methodのところを丹念に読みますと、奇妙なことが時々あります。具体例を一つ挙げてみます。
JAMAの論文です。この論文では、23種類の有害事象がSCRIデザインの手法(リスク期間とコントロール期間の発生率を比較する手法)で分析されました。リスク期間は接種後1~21日(グラフ:A)でした。次に、心筋炎のみが補足解析されました。 リスク期間は接種後0~7日(グラフ:B)でした。
問題は、最初の分析で、リスク期間を、接種後0~20日ではなく、 なぜ接種後1~21日にしたかという点です。
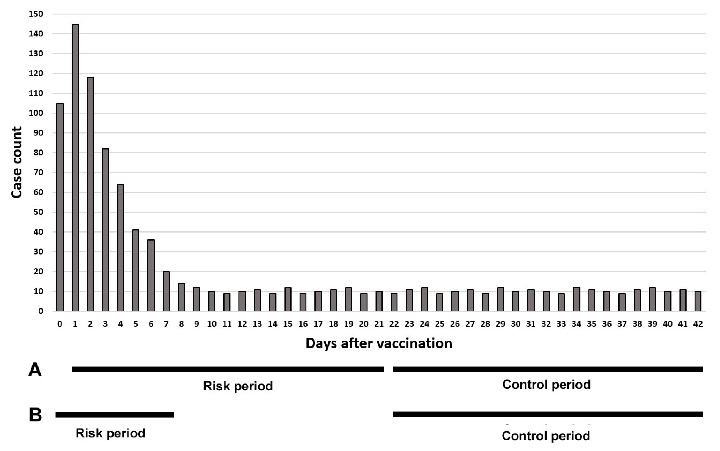
グラフ(※人工的に作成)を見れば一目瞭然ですが、急性期に発症する有害事象の場合には、リスク期間に接種後0日を含めた方が有意差が認められる確率が高くなるわけです。論文には、最初の分析で接種後0日を含めなかった理由は全く記述されていませんでした。
もし、最初の分析で接種後0日を含めて分析しますと、23種類の有害事象のどれかで有意差が認められていたのかもしれません。その事実を隠蔽するために、リスク期間に接種後0日を含めなかったことが推測されます。
これはあくまでも推測であり、本当のことは論文の著者にしか分かりません。隠蔽の疑惑を持たれないためには、不自然なリスク期間の設定をするべきではありません。
バイアス補正が不十分なことを指摘することも有用
全身状態の悪い人の割合に関するバイアスは、一流雑誌に掲載された論文でも必ずしも補正されていません。Takeuchiらの論文においては、このバイアスを補正するために診療報酬明細書を用いました。しかし、明細書には病名は記載されていますが、その重症度は記載されていません。そのため、バイアス補正は十分とは言えません。そのため、この論文では、接種群の死亡率は未接種群の死亡率の約4分の1という実に奇妙な結果となりました。
接種群ではコロナワクチンによる死亡が少ないから死亡率が低くなったのではなく、接種群において全身状態の悪い人の割合が小さいため死亡率が低くなった可能性があるわけです。この問題も英語論文で指摘しました。
最後に、番外の基礎研究(動物実験、In vitro研究)について言及しておきます。勘違いしている人が多い気がしますが、基礎研究のエビデンスレベルは高くありません。参考資料では、最低ランクのレベルにしている資料もあります。つまり、基礎研究の結果のみで因果関係を評価することは適切ではないのです。
基礎研究より、「血栓が発生するリスクがある」といった予測をすることが可能ですが、本当にそうなのかはレベル3以上の研究で確認するしかありません。人体の病態生理は複雑ですので、基礎研究の予想通りに必ずなるわけではないのです。
なお、基礎研究のエビデンスレベルが低いことは、研究の価値が低いことを意味しているわけではありません。むしろ、研究としての価値は非常に高いと私は考えます。あくまでも、エビデンスレベルで見た場合にはそのレベルは低いというだけの話です。
【追記、2025.11.25】
エビデンスピラミッドについて補足しておきます。
・質の低いランダム化比較試験(RCT)よりも、適切にバイアス補正が行われた大規模コホート研究の方が信頼できる場合がある。
・RCTはコホート研究に比べてサンプルサイズが小さいことが多く、まれな有害事象のリスクを検出することは困難である。
・メタアナリシスでは、一次研究の質にばらつきがある場合、結論の信頼性に問題が残る。
・メタアナリシスでは、出版バイアスを補正することは困難である。
したがって、「メタアナリシス>RCT>コホート研究」と単純に序列することが常に適切であるとは言えない。
以上より、エビデンスピラミッドは、以下のように考えた方が実践的ではないかと、私は考えます。